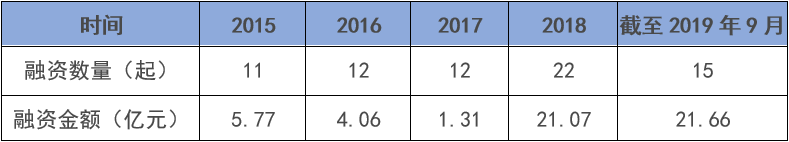
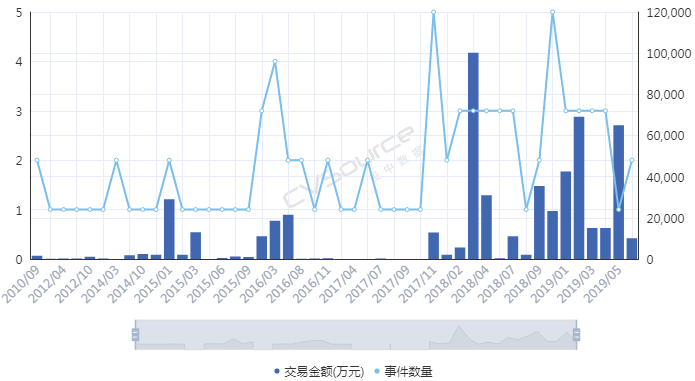
歷經(jīng)寒冬之后�����,細(xì)胞免疫治療正在迎來(lái)資本的蜂擁而入�����。今年以來(lái),截至9月20日�����,中國(guó)細(xì)胞免疫治療行業(yè)融資金額接近22億元�����,已超去年全年�����,是2016年的5倍多,更是2017年的近17倍�����,顯示資本熱情高漲�����。此外�����,這個(gè)月初�����,擁有中國(guó)首款I(lǐng)ND批件且為目前唯一獲準(zhǔn)進(jìn)入實(shí)體瘤治療2期臨床試驗(yàn)細(xì)胞免疫治療產(chǎn)品的永泰生物擬赴港上市�����,更是讓身在其中的企業(yè)和投資機(jī)構(gòu)看到了希望�����。投資人士認(rèn)為�����,隨著全球兩款CAR-T產(chǎn)品獲批上市和國(guó)內(nèi)政策監(jiān)管逐步規(guī)范化,細(xì)胞免疫治療將迎來(lái)新的發(fā)展機(jī)遇�����。但是寒冬過后�����,細(xì)胞免疫治療就會(huì)迎來(lái)春天嗎�����?目前�����,美國(guó)與中國(guó)是開發(fā)細(xì)胞免疫治療產(chǎn)品最為活躍的兩個(gè)國(guó)家�����。美國(guó)專業(yè)期刊《Nature Reviews Drug Discovery》在今年5月發(fā)布的報(bào)告顯示�����,美國(guó)與中國(guó)擁有獲批與在研的細(xì)胞免疫治療產(chǎn)品數(shù)量分別超過了400與300個(gè)�����,合計(jì)約占總數(shù)的四分之三�����。該報(bào)告還指出�����,中國(guó)目前的細(xì)胞免疫治療有47%由生物技術(shù)公司所開發(fā)�����,這一數(shù)字相較去年的38%有明顯增長(zhǎng)�����,中國(guó)的細(xì)胞免疫治療行業(yè)基本形成生物企業(yè)與科研院所平分秋色的局面�����。這反映出中國(guó)細(xì)胞免疫治療產(chǎn)業(yè)的快速發(fā)展�����,背后當(dāng)然也離不開資本的助力。據(jù)CVSources投中數(shù)據(jù)�����,自2018年以來(lái)資本快速涌入細(xì)胞免疫治療行業(yè)�����。2018年全年融資事件達(dá)到22起的歷史最高�����,涉及金額約21.07億元�����,相較2017年披露金額暴增超過15倍�����;今年以來(lái)截至9月20日�����,融資事件雖然僅有15起�����,但融資金額高達(dá)近21.66億元�����,已超去年全年�����,是2016年的5.33倍�����,更是2017年的16.53倍�����。
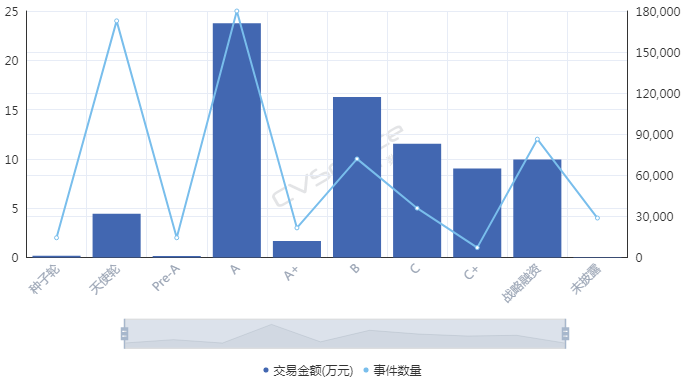
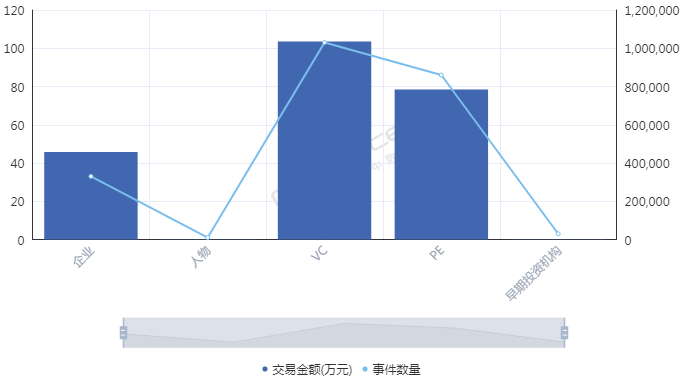
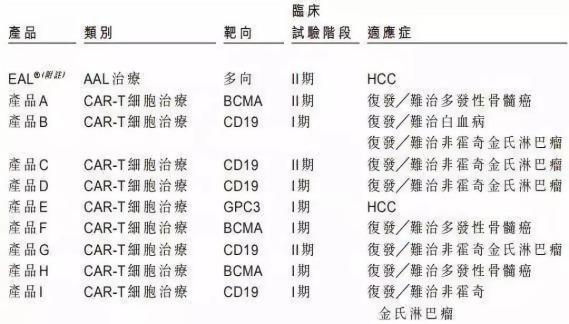
因?yàn)橐黄鸨娝苤氖录?����,?xì)胞免疫治療在2017年遭遇資本寒冬。而后�����,直到2018年初前后�����,融資數(shù)量和金額才先后創(chuàng)出新高�����。從融資進(jìn)度來(lái)看�����,近十年來(lái)進(jìn)入細(xì)胞免疫治療行業(yè)的資本集中在A輪�����,25起融資金額達(dá)到17.11億元�����,B輪和C輪分別以11.72億元�����、8.31億元位列其后�����;天使輪雖然達(dá)到24起�����,僅次于A輪�����,但融資總額僅有3.20億元�����。這也間接顯示出細(xì)胞治療產(chǎn)業(yè)尚處于發(fā)展初期�����,除了因遭遇寒冬之外�����,在一定程度上也跟企業(yè)成立時(shí)間較短有關(guān),多數(shù)企業(yè)成立時(shí)間位于2013年以后�����。那么�����,哪路資本最熱衷于細(xì)胞免疫治療行業(yè)�����?統(tǒng)計(jì)數(shù)據(jù)發(fā)現(xiàn)�����,近十年來(lái)�����,VC和PE成為兩大投資主力�����,其中VC以103起�����,103.53億元的投資金額名列前茅,PE則以86起�����,78.40億元的金額次之�����;多家知名機(jī)構(gòu)�����,如淡馬錫�����、軟銀中國(guó)資本�����、禮來(lái)亞洲基金�����、鼎暉投資�����、君聯(lián)資本�����、深創(chuàng)投等紛紛進(jìn)場(chǎng)�����,不過這些機(jī)構(gòu)多輪跟投的情況并不多見�����。資本為何會(huì)在近兩年對(duì)細(xì)胞免疫治療行業(yè)表現(xiàn)出更大的興趣�����?高特佳投資集團(tuán)創(chuàng)始人�����、董事長(zhǎng)蔡達(dá)建表示�����,國(guó)際上CAR-T產(chǎn)品接連獲批上市和藥監(jiān)局細(xì)胞制品相關(guān)政策的發(fā)布,意味著行業(yè)真正迎來(lái)了全新時(shí)代�����。高特佳曾在去年參與了上海斯丹賽生物技術(shù)有限公司B輪1.8億元的融資�����,該公司成立于2009年�����,主要從事細(xì)胞治療�����、干細(xì)胞和基因編輯等領(lǐng)域�����。此外�����,企業(yè)也是不可忽視的一支投資力量�����,前述同期投資事件合計(jì)達(dá)到33起�����,合計(jì)投資規(guī)模45.81億元�����。A股市場(chǎng)也一度形成了近20家上市公司組成的細(xì)胞免疫治療概念股�����。與VC和PE等投資機(jī)構(gòu)所不同的是�����,企業(yè)進(jìn)入細(xì)胞免疫治療行業(yè)還存在完善公司業(yè)務(wù)布局的意圖�����。此前耗資1.75億元參與上海細(xì)胞治療集團(tuán)有限公司三輪融資的姚記科技就表示,公司持續(xù)看好該公司發(fā)展前景�����,同時(shí)這項(xiàng)投資也有利于完善公司產(chǎn)業(yè)鏈結(jié)構(gòu)和布局�����。有意思的是�����,在國(guó)內(nèi)資本處于低谷的2017年�����,卻被業(yè)界普遍視為細(xì)胞免疫治療的元年�����。這一年的8月和10月�����,諾華制藥和凱特制藥的兩款CAR-T產(chǎn)品(分別為Kymriah�����、Yescarta)先后獲得美國(guó)FDA批準(zhǔn)上市�����,意味著細(xì)胞免疫治療開啟商業(yè)化元年�����。這也使得全球?qū)?xì)胞免疫療法的熱情快速升溫�����,其研發(fā)管線規(guī)模已在整個(gè)腫瘤免疫療法領(lǐng)域雄踞榜首�����,免疫療法甚至還被視為繼放化療�����、手術(shù)�����、靶向治療之后的第四種抗癌方式。據(jù)《Nature Reviews Drug Discovery》報(bào)告�����,截至今年3月�����,全球范圍內(nèi)共有1011款已獲批或正在研發(fā)之中的細(xì)胞免疫療法�����,相較去年同期增加258個(gè)�����;其中CAR-T療法超過五成�����,共有568款�����,相較截至2018年3月增加164個(gè)�����,反映出業(yè)界對(duì)于CAR-T療法的巨大熱情�����。除了首款和第二款CAR-T產(chǎn)品的上市�����,美國(guó)制藥巨頭吉利德科學(xué)在2017年以現(xiàn)金119 億美元收購(gòu)凱特藥業(yè)�����,以及復(fù)星醫(yī)藥牽手凱特藥業(yè)�����、獲得國(guó)內(nèi)首個(gè)CAR-T療法臨床批件的南京傳奇和美國(guó)強(qiáng)生合作等等�����,都顯示出業(yè)界對(duì)細(xì)胞免疫療法的青睞�����。據(jù)永泰生物招股書數(shù)據(jù),截至今年8月�����,我國(guó)共有十種細(xì)胞免疫治療產(chǎn)品處于臨床�����,其中三款產(chǎn)品處于臨床2期�����,尚未有上市或提交NDA的細(xì)胞免疫治療產(chǎn)品�����。值得一提的是�����,全球首款CAR-T產(chǎn)品Kymriah的臨床申請(qǐng)也已于今年8月獲得藥審中心受理�����。截至今年8月我國(guó)處于臨床的十種細(xì)胞免疫治療產(chǎn)品 資料來(lái)源:永泰生物招股書細(xì)胞免疫治療遭遇追捧的背后是未來(lái)可期的市場(chǎng)空間�����。眾所周知�����,癌癥已成為全球第二大死因�����,在中國(guó)則是第一大殺手�����。據(jù)世衛(wèi)組織報(bào)告�����,2018年全球預(yù)計(jì)有1810萬(wàn)癌癥新發(fā)病例和960萬(wàn)癌癥死亡病例(全球所有年齡段�����、性別�����,包括非黑色素瘤皮膚癌在內(nèi)的所有癌癥發(fā)病比例的推算數(shù)據(jù));其中中國(guó)癌癥發(fā)病率�����、死亡率居全球第一�����,在2018年全球癌癥新發(fā)病例和死亡病例中�����,中國(guó)分別占到21%�����、24%�����,且中國(guó)的癌癥治愈率遠(yuǎn)低于美國(guó)等發(fā)達(dá)國(guó)家�����。這些將為癌癥免疫治療未來(lái)的增長(zhǎng)空間提供基礎(chǔ)�����。正如巴黎第六大學(xué)的免疫學(xué)家 David Klatzammn 曾經(jīng)這樣公開評(píng)價(jià):“細(xì)胞免疫療法是一個(gè)極其瘋狂的領(lǐng)域�����,競(jìng)爭(zhēng)激烈�����,未來(lái)發(fā)展值得期待�����?����!?/span>據(jù)弗若斯特沙利文報(bào)告,全球癌癥免疫治療市場(chǎng)規(guī)模將從2018年的206億美元達(dá)到2023年的755億美元�����,中國(guó)將從人民幣19億元達(dá)到人民幣824億元�����;其中中國(guó)的細(xì)胞免疫治療市場(chǎng)規(guī)模預(yù)計(jì)將在2021年至2023年由人民幣13億元升至人民幣102億元���,隨著更多細(xì)胞免疫治療產(chǎn)品獲批��,2030年將達(dá)人民幣584億元����,即2021年至2030年的復(fù)合年增長(zhǎng)率高達(dá)近53%�����,增長(zhǎng)可謂迅猛����。細(xì)胞免疫治療是癌癥免疫治療的主要類型之一(其他類型還包括檢查點(diǎn)抑制劑、治療性癌癥疫苗����、細(xì)胞因子治療等),通俗來(lái)講其治療機(jī)制是將患者血液或腫瘤組織的免疫細(xì)胞(多數(shù)為T細(xì)胞)提取出來(lái)����,通過技術(shù)手段裝上“GPS”后再注回患者體內(nèi),從而對(duì)腫瘤細(xì)胞形成定位打擊。國(guó)內(nèi)外諸多研究顯示���,免疫療法能夠提供相對(duì)持久和更高的緩解���,在預(yù)防腫瘤復(fù)發(fā)方面具有顯著優(yōu)勢(shì)�,從而延長(zhǎng)患者生存期,同時(shí)在某些晚期癌癥患者中通常具有良好的安全性及有效性����,可以規(guī)避傳統(tǒng)的放化療、手術(shù)等方式的弊端(如放化療容易敵我不分造成正常細(xì)胞一定損傷從而引起多種毒副作用�,手術(shù)對(duì)處理早期腫瘤存在局限性等)。2013年癌癥免疫治療被《科學(xué)》雜志列為年度十大科學(xué)突破之首�����,美日兩名免疫學(xué)家也因在腫瘤免疫領(lǐng)域做出的貢獻(xiàn)而獲得2018年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)��,無(wú)不顯示了業(yè)內(nèi)對(duì)免疫療法的認(rèn)可�����。另外�,增強(qiáng)抗腫瘤免疫力的聯(lián)合療法已經(jīng)成為整個(gè)癌癥界非常感興趣的領(lǐng)域,但目前尚未有突破性進(jìn)展。永泰生物在招股書中援引弗若斯特沙利文的報(bào)告稱�,預(yù)計(jì)中國(guó)細(xì)胞免疫治療的研究將進(jìn)一步多樣化,除了將探索更多適應(yīng)癥���,開展免疫療法和其他療法的聯(lián)合治療也將會(huì)是一大趨勢(shì)�����。研究表明���,與采用單一常規(guī)療法相比,聯(lián)合療法可以帶來(lái)更好的臨床效果��。不過�����,細(xì)胞免疫治療仍面臨諸多挑戰(zhàn)和限制��。首先必須看到��,細(xì)胞免疫治療雖然在部分腫瘤類型方面具有顯著療效����,但也存在B面。當(dāng)下最為熱門的CAR-T療法曾經(jīng)挽救了患有急性淋巴性白血病的Emily Whitehead(世界上首個(gè)接受CAR-T療法的兒童)的生命,但其也存在細(xì)胞因子風(fēng)暴��、神經(jīng)毒性和B細(xì)胞缺失等毒副作用�����。由于目前細(xì)胞免疫治療在臨床應(yīng)用方面尚不普遍���,臨床試驗(yàn)面臨患者數(shù)量限制����,部分腫瘤尤其是在實(shí)體腫瘤方面的有效性和安全性難以充分驗(yàn)證�,國(guó)內(nèi)大眾認(rèn)知也不夠充分�����。北京某三甲醫(yī)院專家表示���,雖然免疫治療在我國(guó)比較火熱����,但患者往往是在傳統(tǒng)手段無(wú)法得到有效治療后才有可能進(jìn)行嘗試��。近年來(lái)發(fā)生的多起相關(guān)死亡事件在一定程度上就暴露出細(xì)胞免疫療法在臨床應(yīng)用和試驗(yàn)階段的安全性問題。其次�,細(xì)胞免疫治療并不是“萬(wàn)能神藥”。據(jù)前述專家介紹�����,細(xì)胞免疫治療適應(yīng)癥有限�,國(guó)內(nèi)外在許多實(shí)體腫瘤類型方面并沒有開展試驗(yàn)。然而數(shù)據(jù)顯示�,實(shí)體腫瘤占所有癌癥病例的比例超過90%,也就是說(shuō)細(xì)胞免疫治療在最為核心的實(shí)體腫瘤領(lǐng)域發(fā)揮的效力有限�����。永泰生物在招股書中也稱�����,CAR-T療法在白血病�、非霍奇金淋巴瘤等方面具有顯著功效,但也存在治療后復(fù)發(fā)率較高����、實(shí)體瘤適應(yīng)癥有限的局限性。在國(guó)內(nèi)處于臨床的十種細(xì)胞免疫治療產(chǎn)品中�����,僅有兩種用于治療實(shí)體瘤,而有七種產(chǎn)品用于治療血液系統(tǒng)癌癥����。同時(shí),從研發(fā)競(jìng)爭(zhēng)情況看���,目前細(xì)胞免疫療法主要集中在CD19靶向和CAR-T領(lǐng)域���,未來(lái)這可能會(huì)造成冗余和過度市場(chǎng)競(jìng)爭(zhēng)。據(jù)前述《Nature Reviews Drug Discovery》報(bào)告�����,目前全球共有142款療法針對(duì)CD19�����,占據(jù)總數(shù)的14%�����,其中130款為CAR-T療法�;國(guó)內(nèi)同樣也不例外,十種臨床產(chǎn)品中有九款為CAR-T細(xì)胞產(chǎn)品���,一半為CD19靶點(diǎn)���。細(xì)胞免疫治療未來(lái)若想有更大突破,還需在其他靶點(diǎn)和領(lǐng)域發(fā)力���。另外�����,價(jià)格也有可能會(huì)是一大痛點(diǎn)�����。參考Kymriah和Yescarta分別高達(dá)47.5萬(wàn)美元����、37.3萬(wàn)美元的費(fèi)用����,昂貴的價(jià)格可能會(huì)讓許多患者望而卻步。這些因素都會(huì)影響到細(xì)胞免疫治療的臨床應(yīng)用和市場(chǎng)空間�。監(jiān)管逐步規(guī)范 標(biāo)準(zhǔn)尚未統(tǒng)一對(duì)于資本而言�,吸引其進(jìn)入細(xì)胞免疫治療這個(gè)行業(yè)的動(dòng)力不僅在于可期的市場(chǎng)空間�����,另一大因素還在于趨于規(guī)范的行業(yè)監(jiān)管�。實(shí)際上,細(xì)胞免疫療法在中國(guó)雖然并不是新鮮事物����,國(guó)內(nèi)已有約20年的經(jīng)驗(yàn),但長(zhǎng)期存在法規(guī)盲點(diǎn)�����,很大程度上阻礙了行業(yè)的規(guī)范發(fā)展和應(yīng)用推廣���。2016年5月����,國(guó)家衛(wèi)計(jì)委(現(xiàn)為國(guó)家衛(wèi)健委)緊急叫停醫(yī)療機(jī)構(gòu)在細(xì)胞免疫治療方面的臨床應(yīng)用����,僅允許其作臨床研究���,不得開展收費(fèi)治療��。當(dāng)年12月�,國(guó)家食藥監(jiān)局(原CFDA,現(xiàn)為國(guó)家藥監(jiān)局)發(fā)布了《細(xì)胞制品研究與評(píng)價(jià)技術(shù)指導(dǎo)原則》(征求意見稿)����,首次明確提出將細(xì)胞免疫治療產(chǎn)品納入藥品監(jiān)管;2017年底原CFDA正式發(fā)布《細(xì)胞免疫治療產(chǎn)品與評(píng)價(jià)技術(shù)指導(dǎo)原則》(試行)���,對(duì)其適用的細(xì)胞治療產(chǎn)品范圍進(jìn)行了限定��,并對(duì)細(xì)胞免疫治療產(chǎn)品的藥學(xué)研究����、非臨床研究���、臨床研究等進(jìn)行了規(guī)定��。業(yè)內(nèi)人士認(rèn)為�����,這基本上明確了細(xì)胞免疫治療產(chǎn)品按照藥品監(jiān)管的路徑�����,行業(yè)逐步進(jìn)入從放到收的規(guī)范化軌道�。
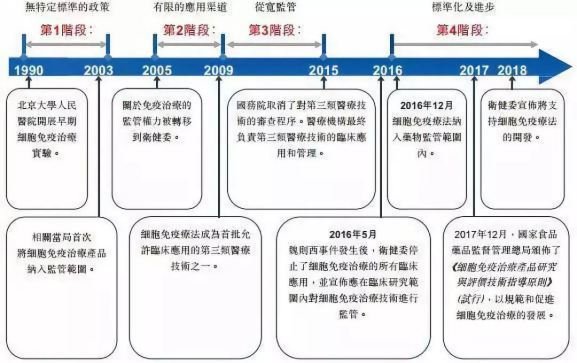
細(xì)胞免疫治療的政策監(jiān)管變化 資料來(lái)源:永泰生物招股書盡管如此,關(guān)于細(xì)胞免疫治療的糾紛和爭(zhēng)議從未停止���。公開信息顯示���,僅僅是2017年國(guó)內(nèi)就發(fā)生過兩起接受免疫療法的患者死亡的案例。難以統(tǒng)一的監(jiān)管和標(biāo)準(zhǔn)被視為這一問題的根源���。2018年國(guó)家衛(wèi)健委宣布將支持開展醫(yī)療機(jī)構(gòu)細(xì)胞免疫療法的臨床����。今年3月底��,經(jīng)國(guó)家藥監(jiān)局同意��,國(guó)家衛(wèi)健委發(fā)布了《體細(xì)胞治療臨床研究和轉(zhuǎn)化應(yīng)用管理辦法(試行)》(征求意見稿)���,旨在規(guī)范和促進(jìn)體細(xì)胞治療臨床研究及轉(zhuǎn)化應(yīng)用,意味著醫(yī)療機(jī)構(gòu)開展細(xì)胞療法臨床研究并從事收費(fèi)治療的大門有望重新開啟���。但是根據(jù)該管理辦法���,醫(yī)療機(jī)構(gòu)備案后即可進(jìn)行臨床研究�、轉(zhuǎn)化應(yīng)用即可收費(fèi)����、限定三甲醫(yī)院開展等規(guī)定引發(fā)業(yè)內(nèi)貶褒不一,尤其是醫(yī)療機(jī)構(gòu)相對(duì)寬松的監(jiān)管標(biāo)準(zhǔn)����,引發(fā)按照藥品監(jiān)管路徑而需要耗費(fèi)更高成本的企業(yè)諸多不滿。目前�����,這一管理辦法尚未正式出臺(tái)實(shí)施����。可見,目前對(duì)細(xì)胞免疫治療的監(jiān)管和標(biāo)準(zhǔn)尚未達(dá)成統(tǒng)一共識(shí)�����,細(xì)胞免疫治療的兩面性(即提取、處理和回輸免疫細(xì)胞的過程可視為診療行為��,但也可將在體外處理的細(xì)胞視為特殊的生物藥品)導(dǎo)致了定義的不同�,進(jìn)而決定了應(yīng)用和監(jiān)管主體的差異。若定義為藥品����,則應(yīng)由藥企主導(dǎo),由藥監(jiān)部門監(jiān)管����;若定義為診療行為,則應(yīng)由醫(yī)院主導(dǎo)����,由衛(wèi)健部門監(jiān)管。明顯的是��,關(guān)于細(xì)胞免疫治療的屬性依舊處于拉鋸狀態(tài)�,政策的天平同樣來(lái)回?fù)u擺。但從目前的政策走向來(lái)看��,細(xì)胞免疫治療行業(yè)將會(huì)形成藥企與醫(yī)院共同主導(dǎo)����、國(guó)家藥監(jiān)局與衛(wèi)健委雙軌監(jiān)管的格局���。這引發(fā)了擔(dān)憂,復(fù)星凱特生物科技有限公司CEO王立群此前曾公開表示��,“雙軌制監(jiān)管可能會(huì)導(dǎo)致行業(yè)質(zhì)量標(biāo)準(zhǔn)以及臨床研究規(guī)范的混淆����,影響行業(yè)的規(guī)范化健康發(fā)展��?��!彼J(rèn)為�����,對(duì)于患者而言�,只有在嚴(yán)格監(jiān)管下才能保障臨床的安全和有效����。不過,也有業(yè)內(nèi)人士認(rèn)為�����,雙軌監(jiān)管并不可怕,關(guān)鍵是要做好分類���,讓藥品的歸為藥監(jiān)部門�����,讓醫(yī)療的歸衛(wèi)生部門����,但必須統(tǒng)一監(jiān)管標(biāo)準(zhǔn)����。目前來(lái)看,統(tǒng)一監(jiān)管可能性不大��,而統(tǒng)一標(biāo)準(zhǔn)或依舊尚需時(shí)日�。