中國國家藥監(jiān)局(NMPA)官網(wǎng)今日公示,由澤璟制藥研發(fā)的1類創(chuàng)新藥甲苯磺酸多納非尼片正式獲批��,用于既往未接受過全身系統(tǒng)性治療的不可切除肝細(xì)胞癌患者。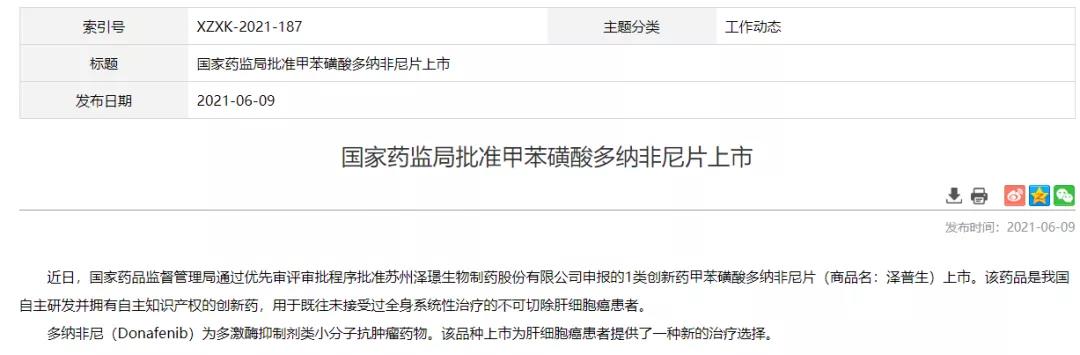
甲苯磺酸多納非尼片是一款口服、多靶點(diǎn)小分子抗腫瘤藥物��。臨床前研究證實(shí)�����,該藥物既可抑制VEGFR�、PDGFR等多種受體酪氨酸激酶的活性,也可直接抑制各種Raf激酶�,并抑制下游的Raf/MEK/ERK信號(hào)傳導(dǎo)通路,抑制腫瘤細(xì)胞增殖和腫瘤血管的形成���,從而發(fā)揮多重抑制、多靶點(diǎn)阻斷的抗腫瘤作用���。2020年5月�,澤璟制藥提交了甲苯磺酸多納非尼的新藥上市申請�����,并于同年10月被納入優(yōu)先審評。據(jù)悉�,該上市申請主要是基于一項(xiàng)名為ZGDH3的臨床研究結(jié)果。ZGDH3是一項(xiàng)開放����、隨機(jī)、平行對照�����、多中心的2/3期臨床研究���,由中國臨床腫瘤學(xué)會(huì)(CSCO)副理事長秦叔逵教授主導(dǎo)���,旨在探索多納非尼片在晚期肝細(xì)胞癌患者一線治療中的有效性與安全性。研究主要終點(diǎn)為總生存期(OS)���,次要終點(diǎn)包括無進(jìn)展生存時(shí)間(PFS)��、客觀緩解率��、疾病控制率(DCR)��、安全性及耐受性等指標(biāo)����。試驗(yàn)結(jié)果顯示,ZGDH3研究達(dá)到了預(yù)設(shè)的主要終點(diǎn)和統(tǒng)計(jì)學(xué)要求����。在未接受過系統(tǒng)治療的不可手術(shù)或轉(zhuǎn)移性晚期肝細(xì)胞癌患者中,多納非尼治療組的中位總生存期(mOS)顯著優(yōu)于對照藥物治療組�,達(dá)到統(tǒng)計(jì)學(xué)上差異顯著性且具有臨床意義的延長。此外�����,多納非尼組在3級及以上不良事件發(fā)生率��、與藥物相關(guān)的導(dǎo)致停藥或減量的不良事件發(fā)生率等方面顯示出更優(yōu)的安全性�。除了肝癌之外,澤璟制藥還在開展多納非尼治療晚期結(jié)直腸癌和甲狀腺癌的關(guān)鍵性臨床研究���,同時(shí)也在積極推進(jìn)多納非尼聯(lián)合PD-1/PD-L1單抗治療多種腫瘤的新型研究����。祝賀甲苯磺酸多納非尼片在中國獲批��,期待這款藥物可以為需要的病患帶來福音��。



