8月17日,中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心(CDE)最新公示,由復(fù)星凱特申報(bào)的阿基侖賽注射液被納入突破性治療藥物程序�,擬用于治療接受過(guò)二線或以上系統(tǒng)治療后復(fù)發(fā)或難治性惰性非霍奇金淋巴瘤�����。這是繼今年6月阿基侖賽在中國(guó)獲批上市之后�,該產(chǎn)品近期迎來(lái)的又一重要進(jìn)展��。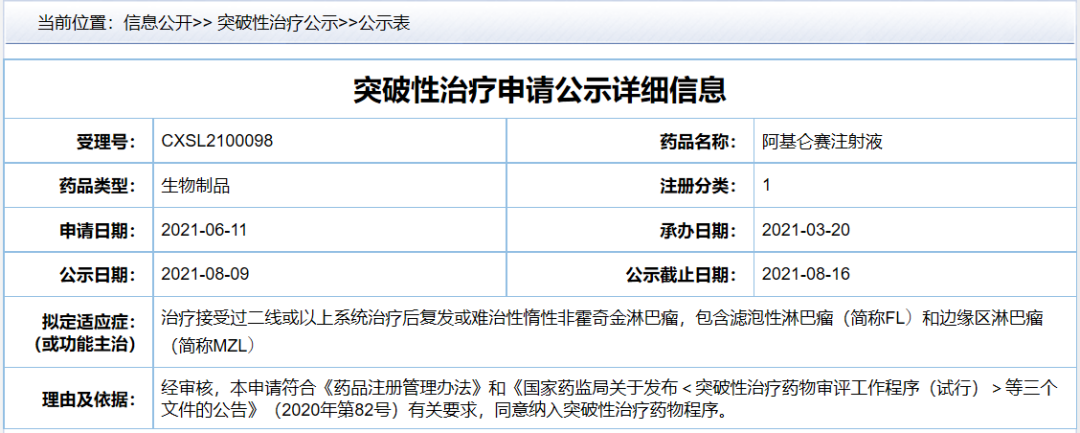
阿基侖賽注射液(代號(hào):FKC876)是復(fù)星凱特于2017年從吉利德科學(xué)(Gilead Sciences)旗下公司Kite引進(jìn)Yescarta(Axicabtagene Ciloleucel)����、進(jìn)行技術(shù)轉(zhuǎn)移、并獲授權(quán)在中國(guó)進(jìn)行本地化生產(chǎn)的靶向CD19自體CAR-T細(xì)胞治療產(chǎn)品。CAR-T免疫細(xì)胞治療是通過(guò)基因工程修飾患者自體T細(xì)胞�,以表達(dá)靶向腫瘤抗原的嵌合抗原受體分子,由激活的T細(xì)胞介導(dǎo)殺傷腫瘤細(xì)胞�。6月22日,復(fù)星凱特宣布阿基侖賽注射液(商品名:奕凱達(dá))已正式在中國(guó)獲批上市�,用于治療既往接受二線或以上系統(tǒng)性治療后復(fù)發(fā)或難治性大B細(xì)胞淋巴瘤(r/r LBCL)成人患者。這是首個(gè)且目前唯一獲中國(guó)國(guó)家藥監(jiān)局批準(zhǔn)的CAR-T產(chǎn)品����,這一批準(zhǔn)也意味著中國(guó)正式邁入CAR-T細(xì)胞治療的新時(shí)代����。

此次阿基侖賽注射液在中國(guó)被納入突破性治療藥物程序,擬用于治療復(fù)發(fā)或難治性惰性非霍奇金淋巴瘤�,且接受過(guò)二線或以上系統(tǒng)治療的患者,包含濾泡性淋巴瘤(FL)和邊緣區(qū)淋巴瘤(MZL)患者���。FL和MZL均為惰性NHL����,患者的惡性腫瘤生長(zhǎng)緩慢�����,但隨時(shí)間推移可變得更具侵襲性。其中�����,F(xiàn)L是最常見(jiàn)的惰性淋巴瘤���,它約占全世界確診的淋巴瘤的22%����。MZL是第三常見(jiàn)的淋巴瘤�,占所有B細(xì)胞NHL的8%-12%。在美國(guó)����,Yescarta也曾被FDA授予這些適應(yīng)癥的突破性療法認(rèn)定。Kite公司于2020年9月向FDA提交了Yescarta的補(bǔ)充生物制品許可申請(qǐng)(sBLA)�,并于2021年3月獲得FDA加速批準(zhǔn),用于治療既往接受過(guò)兩線以上系統(tǒng)性治療的復(fù)發(fā)/難治性濾泡性淋巴瘤患者�����。這一批準(zhǔn)���,使得Yescarta成為第一款獲批用于治療惰性濾泡性淋巴瘤患者的CAR-T產(chǎn)品��。Kite公司本次sBLA的提交基于Yescarta的2期臨床試驗(yàn)ZUMA-5的主要分析結(jié)果��。根據(jù)2020年12月份美國(guó)臨床血液學(xué)會(huì)(ASH)年會(huì)上公布的ZUMA-5分析結(jié)果����,在中位隨訪時(shí)間達(dá)到17.5個(gè)月時(shí),療效可評(píng)估的104例惰性非霍奇金淋巴瘤患者的總緩解率(ORR)達(dá)到92%��,完全緩解率(CR)達(dá)到76%���,其中濾泡淋巴瘤患者的ORR為94%,CR達(dá)到80%���,中位DOR尚未達(dá)到�����,64%的患者在數(shù)據(jù)截止時(shí)仍保持緩解��。ZUMA-5中未發(fā)現(xiàn)新的與Axi-Cel相關(guān)的不良事件����。Kite公司曾在新聞稿中表示�����,惰性NHL患者的疾病開(kāi)始時(shí)進(jìn)展緩慢,但隨著時(shí)間的推移�����,每次復(fù)發(fā)變得更具侵襲性���。在ZUMA-5中觀察到的療效可能為某些類型的惰性NHL高?�;颊咛峁┮环N潛在的變革性治療選擇�。希望復(fù)星凱特的阿基侖賽注射液早日在中國(guó)獲批新適應(yīng)癥�,為更多惰性非霍奇金淋巴瘤帶來(lái)新的治療選擇。



