第40屆JPM醫(yī)療健康大會(huì)進(jìn)入第二天��,今天的這篇文章里��,藥明康德內(nèi)容團(tuán)隊(duì)將繼續(xù)與讀者分享JPM上的最新合作和研發(fā)進(jìn)展����。安進(jìn)與Arrakis合作開發(fā)創(chuàng)新小分子RNA降解劑安進(jìn)和Arrakis Therapeutics宣布達(dá)成研發(fā)協(xié)議,針對(duì)多個(gè)治療領(lǐng)域的難于成藥靶點(diǎn)�,共同發(fā)現(xiàn)和開發(fā)RNA降解劑。這一創(chuàng)新藥物類型是一種小分子藥物�,它通過(guò)將編碼致病蛋白的RNA與核酸酶拉近到一起,導(dǎo)致它們的選擇性降解��。根據(jù)合作協(xié)議���,Arrakis將獲得7500萬(wàn)美元前期付款和可高達(dá)數(shù)十億美元的里程碑付款(詳情請(qǐng)見藥明康德今日推送第4條)��。“我們很高興與安進(jìn)的研究團(tuán)隊(duì)合作���,共同構(gòu)建降解導(dǎo)致疾病RNA的新藥物類型。這一合作進(jìn)一步證明了我們靶向RNA的小分子技術(shù)平臺(tái)的用途�,為給患者帶來(lái)強(qiáng)力新療法鋪平了道路?���!盇rrakis公司首席執(zhí)行官M(fèi)ichael Gilman博士說(shuō)。
▲Arrakis公司首席執(zhí)行官M(fèi)ichael Gilman博士在2019藥明康德全球論壇上分享如何利用顛覆性技術(shù)靶向難于靶向的靶點(diǎn)
Mirati公司向美國(guó)FDA遞交KRAS G12C抑制劑新藥申請(qǐng)Mirati公司高管在JPM大會(huì)的報(bào)告上宣布���,該公司已經(jīng)在去年年底��,完成向美國(guó)FDA遞交其KRAS G12C抑制劑adagrasib的新藥申請(qǐng)���,用于二線治療攜帶KRAS G12C突變的非小細(xì)胞肺癌(NSCLC)患者����。Adagrasib是一款具有差異化特征的強(qiáng)力口服KRAS G12C抑制劑���。在治療攜帶KRAS G12C突變的經(jīng)治NSCLC患者的2期臨床試驗(yàn)中����,它獲得了43%的客觀緩解率(ORR)�,值得一提的是,98.3%接受adagrasib治療的患者���,都已經(jīng)接受過(guò)了免疫療法和化療��,因此對(duì)于這些患者群體而言是一個(gè)新的希望。圖片來(lái)源:Mirati公司官網(wǎng)Mirati預(yù)計(jì)今年將公布adagrasib的療效持久性數(shù)據(jù)和在攜帶大腦轉(zhuǎn)移瘤的患者中的療效數(shù)據(jù)�。Evaluate日前發(fā)布的報(bào)告中將它列為今年有望獲批的潛在重磅療法之一。靶向BCMA和CD22����,Sana達(dá)成兩項(xiàng)細(xì)胞療法研發(fā)合作Sana Biotechnology公司的目標(biāo)之一是開發(fā)體內(nèi)和體外工程化改造的細(xì)胞療法���。在JPM大會(huì)上,該公司宣布達(dá)成了兩項(xiàng)研發(fā)合作����。首先,該公司與馴鹿醫(yī)療和信達(dá)生物達(dá)成協(xié)議�,獲得臨床驗(yàn)證的靶向B細(xì)胞成熟抗原(BCMA)的嵌合抗原受體(CAR)結(jié)構(gòu),用于開發(fā)某些體內(nèi)基因療法和體外細(xì)胞療法����。馴鹿醫(yī)療和信達(dá)生物將獲得前期付款和可高達(dá)2.04億美元的潛在里程碑付款。此外���,該公司今日宣布與美國(guó)國(guó)家癌癥研究所(NCI)達(dá)成協(xié)議��,獲得其開發(fā)的靶向CD22的CAR結(jié)構(gòu)�,用于治療B細(xì)胞惡性腫瘤的體內(nèi)基因療法和體外同種異體CAR-T療法的開發(fā)���。這些療法有望解決經(jīng)靶向CD19的CAR-T療法治療后復(fù)發(fā)的患者面對(duì)的挑戰(zhàn)�。獲羅氏2.9億美元投資��,新銳加快推進(jìn)多組學(xué)早期癌癥檢測(cè)平臺(tái)Freenome公司宣布����,獲得羅氏(Roche)數(shù)額為2.9億美元的投資����,自該公司創(chuàng)建以來(lái)��,總?cè)谫Y數(shù)額已經(jīng)超過(guò)11億美元�。Freenome公司的多組學(xué)平臺(tái)靶向血液中的關(guān)鍵生物信號(hào),對(duì)游離DNA(cfDNA)����,DNA甲基化水平,以及蛋白生物標(biāo)志物進(jìn)行分析���。再與先進(jìn)的計(jì)算生物學(xué)和機(jī)器學(xué)習(xí)技術(shù)相結(jié)合����,對(duì)信息進(jìn)行綜合處理��,識(shí)別與疾病相關(guān)的標(biāo)志物模式�,從而提高早期癌癥篩查的準(zhǔn)確性。該公司用于早期發(fā)現(xiàn)結(jié)直腸癌的血液檢測(cè)目前正在注冊(cè)性臨床研究中接受檢驗(yàn)���。近日����,該公司也匯報(bào)了這一多組學(xué)平臺(tái)在發(fā)現(xiàn)胰腺癌方面的可喜數(shù)據(jù)���。DMD基因療法顯著改善患者運(yùn)動(dòng)功能Sarepta Therapeutics公司在JPM的報(bào)告上公布了用于治療杜氏肌營(yíng)養(yǎng)不良(DMD)的在研基因療法SRP-9001的最新臨床試驗(yàn)數(shù)據(jù)�。此次匯報(bào)的數(shù)據(jù)來(lái)自在隨機(jī)雙盲臨床試驗(yàn)中原來(lái)接受安慰劑治療的患者����,它們?cè)陔p盲期過(guò)后轉(zhuǎn)變?yōu)榻邮躍RP-9001的治療。SRP-9001是一款利用AAV病毒載體���,表達(dá)抗微肌萎縮蛋白的轉(zhuǎn)基因的基因療法���。試驗(yàn)結(jié)果顯示,在這一患者群體中���,接受治療48周后��,與預(yù)先確定的匹配外部對(duì)照群體相比����,用于檢測(cè)運(yùn)動(dòng)能力的NSAA指標(biāo)提高2.0點(diǎn)(p=0.0009)����。羅氏在2019年與Sarepta達(dá)成28.5億美元的研發(fā)合作���,雙方已經(jīng)在去年啟動(dòng)關(guān)鍵性臨床試驗(yàn),將在美國(guó)�、歐洲和亞洲招募患者,檢驗(yàn)這一療法的效果��。利用微RNA沉默多個(gè)基因��,Allogene合作開發(fā)下一代即用型CAR-T細(xì)胞療法Allogene昨天宣布美國(guó)FDA已經(jīng)放行了該公司所有即用型細(xì)胞療法臨床試驗(yàn)�。今日,該公司宣布與Antion Biosciences達(dá)成合作����,將利用其基于微RNA(miRNA)的miCAR技術(shù)平臺(tái),開發(fā)下一代同種異體CAR-T療法��。同種異體CAR-T療法在引入靶向腫瘤抗原的CAR的同時(shí)��,還需要對(duì)來(lái)源于健康供體的T細(xì)胞進(jìn)行一系列改造����,比如抑制內(nèi)源性T細(xì)胞受體的表達(dá),降低患者對(duì)外來(lái)細(xì)胞的免疫排斥,提高療法的持久性等等��。Antion公司的miCAR平臺(tái)在同一載體中��,可以添加多個(gè)微RNA結(jié)構(gòu)���,從而在引入CAR的同時(shí),可沉默多達(dá)6個(gè)基因的表達(dá)�,從而更高效地完成對(duì)T細(xì)胞的改造。
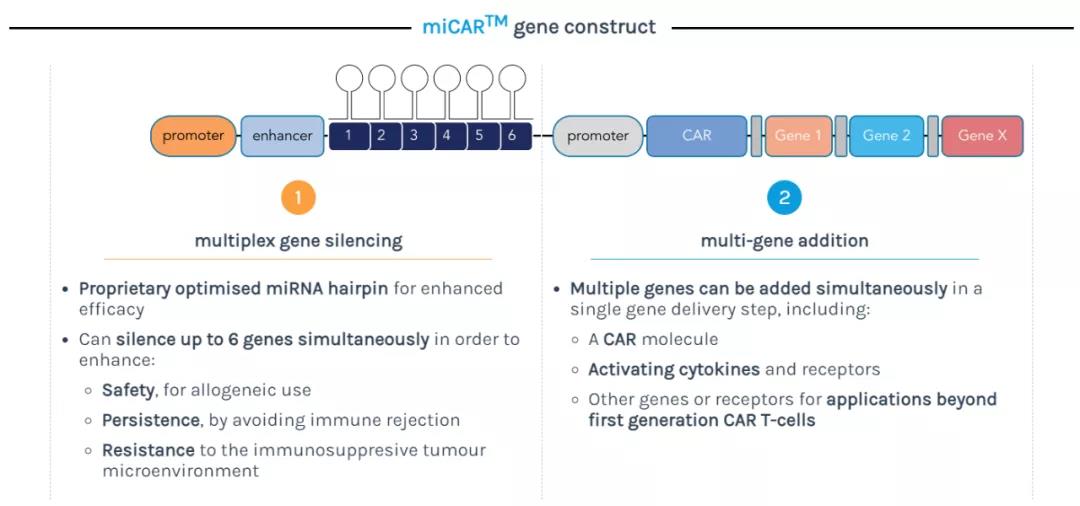
▲miCAR技術(shù)平臺(tái)圖示(圖片來(lái)源:Antion Biosciences公司官網(wǎng))
文章來(lái)源:藥明康德