1月18日,中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心(CDE)公示顯示,Nektar Therapeutics申報(bào)的bempegaldesleukin已獲得臨床試驗(yàn)?zāi)驹S可,擬開(kāi)發(fā)用于頭頸部鱗狀細(xì)胞癌��。公開(kāi)資料顯示����,這是一種靶向IL-2信號(hào)通路的激動(dòng)劑��,曾獲FDA授予突破性療法認(rèn)定,研發(fā)代號(hào)為NKTR-214�。2018年,Nektar公司曾與百時(shí)美施貴寶(BMS)達(dá)成超36億美元的研發(fā)合作����,以全方位研究NKTR-214與BMS管線(xiàn)中多種免疫檢查點(diǎn)抑制劑聯(lián)用在多種癌癥中的治療效果。根據(jù)Nektar公司官網(wǎng)介紹�����,目前雙方正在積極推進(jìn)NKTR-214與nivolumab(Opdivo)的5個(gè)注冊(cè)臨床試驗(yàn)和1個(gè)中期臨床試驗(yàn)�。同時(shí),Nektar公司也正在與德國(guó)默克(Merck KGaA)和SFJ Pharmaceuticals合作開(kāi)發(fā)NKTR-214�����,對(duì)腫瘤表達(dá)PD-L1的轉(zhuǎn)移性頭頸癌患者進(jìn)行的2/3期臨床研究�。
那么NKTR-214(bempegaldesleukin,Bempeg)為何被這么多公司看好呢���?這要從它的作用靶點(diǎn)IL-2說(shuō)起�。IL-2療法是最早獲得批準(zhǔn)用于治療癌癥的免疫療法之一�。作為一種細(xì)胞因子,它具有激活CD8陽(yáng)性T細(xì)胞���,自然殺傷細(xì)胞并且促進(jìn)它們?cè)鲋车哪芰?���,因此曾?jīng)獲得美國(guó)FDA的批準(zhǔn)用于治療黑色素瘤和腎細(xì)胞癌。然而���,IL-2同時(shí)具有激活具有免疫抑制功能的調(diào)節(jié)性T細(xì)胞(Treg)的能力����,這反而會(huì)抑制T細(xì)胞的抗癌免疫反應(yīng)���,而且可能導(dǎo)致其它毒副作用。因此�,IL-2領(lǐng)域的一個(gè)研發(fā)重心是開(kāi)發(fā)能夠在CD8陽(yáng)性T細(xì)胞中選擇性激活I(lǐng)L-2受體信號(hào)通路的激活劑。而NKTR-214正是一款傾向與IL-2信號(hào)通路中的CD122受體相結(jié)合的激動(dòng)劑����,它有望通過(guò)選擇性激活I(lǐng)L-2信號(hào)通路,刺激CD8+效應(yīng)T細(xì)胞�����、天然殺傷細(xì)胞和CD4+輔助T細(xì)胞的增殖���。在治療初治無(wú)法切除或轉(zhuǎn)移性黑色素瘤患者的1/2期臨床試驗(yàn)PIVOT-02中��,NKTR-214與PD-1抑制劑Opdivo構(gòu)成的組合療法達(dá)到53%的客觀緩解率(ORR)����。在中位隨訪(fǎng)時(shí)間為12.7個(gè)月時(shí),完全緩解率達(dá)到34%�,而且隨著隨訪(fǎng)時(shí)間的增加,獲得完全緩解的患者比例也不斷增加��。這表明在出現(xiàn)緩解的患者中�,組合療法帶來(lái)的緩解程度不斷加深。基于這些積極結(jié)果�,F(xiàn)DA授予了NKTR-214與Opdivo組合療法突破性療法認(rèn)定,治療初治無(wú)法切除或轉(zhuǎn)移性黑色素瘤患者�。此外,NKTR-214還獲得FDA授予的孤兒藥資格�,用于治療IIb至IV期黑色素瘤。值得一提的是���,在2021年2月Fierce Pharma和Evaluate聯(lián)合發(fā)布的“2021年最受期待上市的10種藥物”名單中���,NKTR-214也位列榜單。
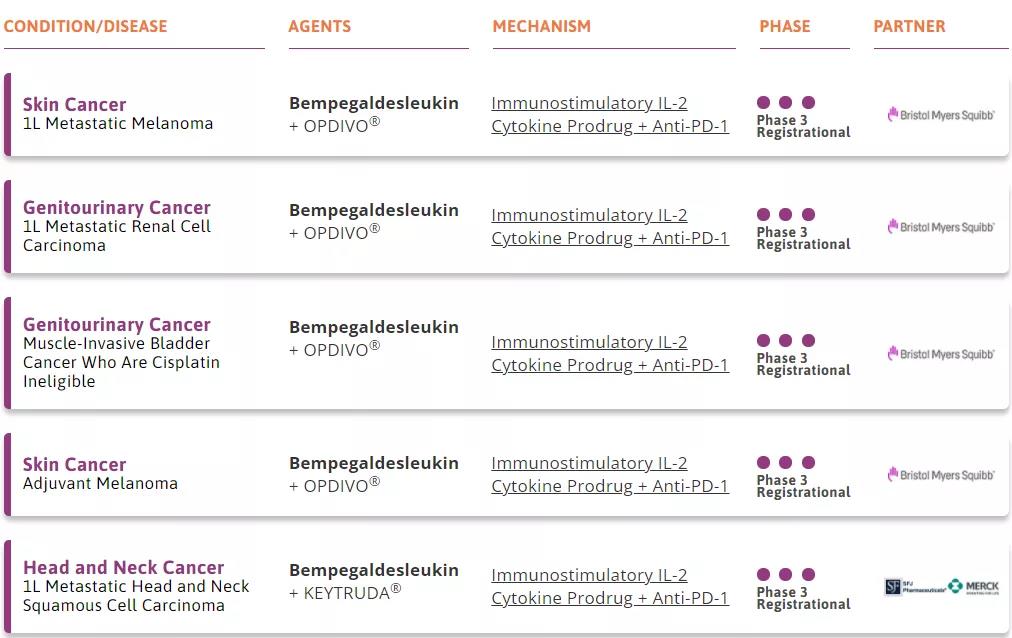
▲NKTR-214正在進(jìn)行多項(xiàng)注冊(cè)臨床試驗(yàn)(截圖來(lái)源:Nektar公司官網(wǎng))
眾所周知���,包括PD-1/PD-L1抑制劑在內(nèi)的免疫檢查點(diǎn)抑制劑雖然在治療多種癌癥方面取得卓越的療效���,但是仍然有很多患者對(duì)這些療法沒(méi)有響應(yīng)���。因此,癌癥免疫療法的重要研究方向之一是找尋免疫檢查點(diǎn)抑制劑的“好幫手”��,構(gòu)建組合療法擴(kuò)展檢查點(diǎn)抑制劑的療效和使用范圍�����。NKTR-214在臨床試驗(yàn)中取得的積極結(jié)果��,意味著這一靶向IL-2信號(hào)通路的激動(dòng)劑在增強(qiáng)免疫檢查點(diǎn)抑制劑療效方面的一個(gè)重要突破����。在中國(guó)���,NKTR-214此前也已獲得CDE臨床試驗(yàn)?zāi)驹S可�����,與Opdivo聯(lián)合治療既往未經(jīng)治療的晚期或轉(zhuǎn)移性腎細(xì)胞癌患者����。此次為該產(chǎn)品再次在中國(guó)獲批開(kāi)展頭頸部鱗狀細(xì)胞癌的臨床試驗(yàn)。希望NKTR-214在這些臨床研究中進(jìn)展順利�����,早日為癌癥患者帶來(lái)新的����、療效更好的治療選擇。
參考資料:
[1]中國(guó)國(guó)家藥監(jiān)局藥品審評(píng)中心. Retrieved Jan 18��,2022, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d[2] The 10 most-anticipated drug launches of 2021 . Retrieved Feb 22, 2021. From https://www.fiercepharma.com/special-report/10-most-anticipated-drug-launches-2021[3] Nektar Therapeutics Presents Biomarker and Clinical Data from PIVOT-02 Phase 2 Study of Bempegaldesleukin with Nivolumab at 2019 ASCO Annual Meeting. Retrieved August 1, 2019, from https://ir.nektar.com/news-releases/news-release-details/nektar-therapeutics-presents-biomarker-and-clinical-data-pivot
文章來(lái)源:醫(yī)藥觀瀾





